康柏西普视网膜静脉阻塞适应证审评顺利
文章图片
文章图片
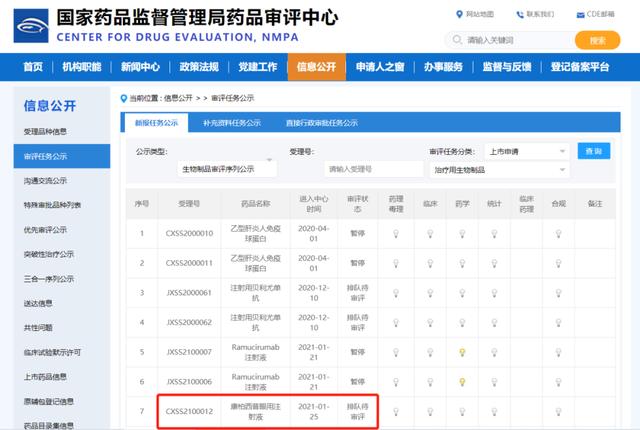
2021年11月29日查询自国家药品监督管理局官网
2014年7月 , 我国自主研发的治疗眼底黄斑变性的国家生物1类新药康柏西普上市 。上市7年来 , 康柏西普创造了诸多奇迹 , 并连续获批湿性年龄相关性黄斑变性、继发于病理性近视的脉络膜新生血管、糖尿病黄斑水肿3个适应证 。当下 , 康柏西普第四个适应证——视网膜静脉阻塞已完成临床研究 , 进入审评阶段 。
康弘药业相关负责人表示 , 康柏西普仍处于并将长期处于发展战略机遇期 , 长期向好的发展趋势没有改变 , 民族品牌的发展韧性依然强劲 。
新适应证获批在望
康柏西普是一种血管内皮生长因子(VEGF)受体与人免疫球蛋白Fc段基因重组的融合蛋白 , 通过结合VEGF , 竞争性抑制VEGF与受体结合并阻止VEGF家族受体的激活 , 能够抑制内皮细胞增殖和血管新生 。
视网膜静脉阻塞是最常见的视网膜疾病之一 , 是一种视网膜血管性疾病 , 多由高血压 , 高血脂 , 糖尿病等疾病引起 , 在眼底疾病中发病率位列第二名 。黄斑囊样水肿、视网膜视盘新生血管、玻璃体出血和新生血管性青光眼是视网膜静脉阻塞常见的并发症 , 可导致患者永久性失明 。
如果康柏西普视网膜静脉阻塞新适应证获批上市 , 不仅可以给视网膜静脉阻塞患者带来新的治疗选择 , 而且也将给黄斑囊样水肿、视网膜视盘新生血管、玻璃体出血和新生血管性青光眼的治疗提供新路径 。这不仅有利于提升创新药物可及性和扩大获益患者人群 , 而且也有利于进一步发挥、挖掘康柏西普的社会价值 。
保障供应属性增强
之前 , 我国眼用抗VEGF药物完全依赖进口 。作为中国眼科领域唯一一个自主研发并在国内成功上市的生物新药 , 康柏西普的问世打破了进口产品市场垄断 。
截至2021年4月 , 围绕康柏西普 , 康弘药业已完成74项临床研究 , 发表1462篇文章 。上市7年来 , 康柏西普累计注射超过180万次 。临床实践与临床研究结果均证明了康柏西普的有效性与安全性 。
康柏西普的临床价值和社会价值得到业内专家的一致肯定 。有专家表示 , 与国外同类产品相比 , 康柏西普具有靶点多、亲和力高、作用时间长等优势 , 能显著提高并高效维持患者视力 , 降低给药频次 , 从而降低患者负担与医疗成本 。
2017年 , 康柏西普被纳入国家医保目录;2018年 , 康柏西普被纳入国家基药目录;2020年 , 康柏西普被纳入《中国药典》 , 进一步增强了其优先使用的保障供应属性 。
此外 , 康柏西普与风云气象卫星、新一代核潜艇、复兴号动车组等国之重器一起荣获第五届工业大奖 , 成为该奖项设立以来第一款获此殊荣的生物药 。中国医药创新促进会会长宋瑞霖曾评价道:“康柏西普是改革开放40周年的显著创新成果 , 折射出的是中国医药工业的整体水平 。

文章图片
文章图片
文:王雨
编辑:王天鹅
审核:韩璐
【康柏西普视网膜静脉阻塞适应证审评顺利】
文章图片
文章图片
来源:健康报
推荐阅读
- 河南省立眼科医院为出生仅30天患儿实施视网膜脱离手术
- 荣昌生物泰它西普、维迪西妥单抗开出首张医保处方
- 广西首例!FCB治疗孔源性视网膜脱离手术在南宁爱尔眼科医院开展
- 市场星报“健康365”与您相约,谈谈“警惕隐蔽的致盲杀手—糖尿病视网膜病变”
- 90后小伙躺着玩手机砸眼致视网膜脱离,医生建议要进行定期的眼底筛查
- PNAS:在哺乳动物视网膜中发现了一种新的神经元类型
- 视网膜脱落是什么原因引起的 造成视网膜脱落的“五大元凶”,你了解吗?
- 西普 西普教育发布U-SaaS在线竞赛训练平台高职版
- 广西普通话 广西人的普通话,这下子在全国又火了!
- 糖尿病患者视网膜发生病变,可能是这5个原因引发的














